
Biossegurança em Biotérios de Experimentação (Parte I)
Articulos Cientificos 15 August 2013Biossegurança em Biotérios de Experimentação
Risco Biológico e níveis de proteção
Parte I - Procedimentos e Práticas
Autor: Joel Majerowicz MV MSc
Os riscos biológicos em biotérios existem porque animais são reservatórios naturais de várias zoonoses e podem, portanto, abrigar ou serem susceptíveis a agentes infecciosos capazes de causar doenças no ser humano. São também produtores de alérgenos e que dependendo da sensibilidade individual da pessoa podem desencadear o desenvolvimento de reação de hipersensibilidade (alergia) e levar a problemas alérgicos de baixa gravidade até doença respiratória grave.
As infecções associadas à experimentação animal é o resultado de numerosos fatores, quais sejam; O agente infeccioso, animais que servem de reservatórios, a susceptibilidade do técnico envolvido no manuseio, uso, observação, manejo ou em outras atividades com a experimentação e manutenção animal.
Se o propósito do uso de animais é o estudo de doença que envolva agente infeccioso, o agente e o reservatório estão presentes. Quando não for o caso, a presença do agente é dependente de infecções ou estado de doença do animal. A utilização de animais obtidos de criações confiáveis e que certifiquem o padrão sanitário dos animais, reduz o potencial de portarem agentes infecciosos. Um período de quarentena apropriado para a realização de testes de diagnóstico e apropriado tratamento, quando possível, auxilia na prevenção de infecções para técnicos e animais.
A susceptibilidade do técnico é dependente do seu estado imunológico. Três fatores adicionais podem estar presentes nas doenças do trabalho: Se ocorre o escape do agente da área de experimentação, se o agente pode ser transmitido para o técnico e se o agente invade o local de trabalho. Métodos para o controle dos riscos biológicos ou práticas de biossegurança são primariamente utilizados. O conhecimento desses fatores, em particular ao agente em que se manipula, auxilia na seleção das medidas de biossegurança apropriadas.
Forma de escape
O agente infeccioso pode escapar por via natural ou artificial. Eliminação do agente pela urina, saliva e fezes ou através de lesões na pele são exemplos de escape natural. Há vários mecanismos de escape artificial, como biópsia, coleta de sangue, tecidos e fluídos corpóreos, necropsia e instrumental cirúrgico contaminado.
Transmissão
A transmissão do agente do animal ou do laboratório pode ocorrer por várias rotas. A mais frequente envolve agulhas e seringas contaminadas e a formação de aerossóis.
Exposição
A inalação, o contato com membranas mucosas e a inoculação parenteral são as formas de exposição mais frequentes. Em situações envolvendo a atividade ocupacional, a exposição pode ser similar ao processo natural ou bem diferente. Como exemplo a Tularemia que normalmente é adquirida por contato das membranas mucosas ou inoculações percutâneas com sangue ou tecidos infectados de coelhos e no laboratório inalações de aerossóis, quando do manuseio de culturas, é o principal meio de transmissão.
Os mecanismos mais comuns de exposição, quando animais de laboratório estão envolvidos são:
-
Inoculação direta por agulhas, contaminação de cortes ou arranhões preexistentes, por instrumentos contaminados e agressão animal;
-
Inalação de aerossóis durante o manejo animal e nos procedimentos e manipulação na experimentação animal;
-
Contato das membranas mucosas dos olhos, boca ou narinas por gotículas de materiais, mãos e superfícies contaminadas;
-
A ingestão é pouco comum, uma vez que as boas práticas laboratoriais coíbem a prática de se “pipetar” com a boca.
As características do animal, o agente infeccioso envolvido, o treinamento e a experiência do pessoal, as atividades e os procedimentos requeridos na experimentação, devem ser considerados na avaliação e seleção das regras de biossegurança. Somente com conscientização e conhecimento das particularidades envolvidas na experimentação animal e que se pode selecionar as normas de biossegurança adequadas, visando minimizar ou até mesmo eliminar os riscos existentes, porém somente com o uso contínuo e por todos os envolvidos é que se obtêm resultados seguros.
Os laboratórios que manipulam microrganismos patogênicos ou que tenham a possibilidade de contê-los no material de trabalho são especiais. Nesses ambientes de trabalho há risco de se contrair doenças infecciosas, tanto pelo pessoal que nele trabalhe, como para os que estão próximos. Com a experiência adquirida ao longo do tempo e com o desenvolvimento das ciências e tecnologias, a diminuição ou mesmo a eliminação dos riscos se torna possível, quando se faz uso de boas técnicas laboratoriais e empregam-se as recomendações de biossegurança específicas ao nível do risco em potencial.
Contenção
São os métodos e técnicas, procedimentos e práticas, equipamentos de proteção individual e coletiva e condições de instalações laboratoriais, que devem ser empregados na manipulação ou estocagem de agentes infecciosos no ambiente laboratorial. A finalidade da contenção é a de eliminar ou reduzir a exposição, ao agente de risco, do pessoal, do laboratorial e do ambiente externo.
Contenção primária
É a proteção individual e do laboratório diante de um agente infeccioso. Essa contenção se efetiva pelo emprego de técnicas laboratoriais e o uso de equipamentos de proteção individual (EPI) e/ou coletivo (EPC).
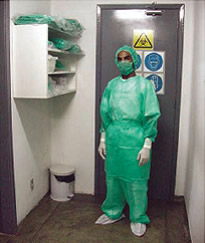
Fig 2. Paramentação (EPI)

Fig 3. Cabine de Segurança biológica (EPC)
Contenção secundária
É a proteção das áreas externas ao laboratório de uma contaminação do agente microbiológico experimental em uso. Essa proteção é dada pelas instalações, sistemas de utilidades prediais e métodos operacionais.
Esses itens de segurança individual e coletivo, bem como as instalações, permitem eliminar ou diminuir os riscos associados a um determinado agente de risco.
Classes de risco

Fig 4. Símbolo de Risco Biológico
O organismo, a ser utilizado no trabalho, será classificado com base no seu potencial patogênico em quatro classes de risco:
-
Classe 1 - Organismo que não cause doença ao homem ou animal;
-
Classe 2 – Microrganismo associado com doença humana ou animal, mas que não consiste em sério risco a quem o manipula, ao ambiente de trabalho e ao meio ambiente. Normalmente a forma de contaminação se dá por auto inoculação, ingestão ou exposição de membranas mucosas;
-
Classe 3 – Microrganismo patogênico que cause doença grave ao homem ou a espécie animal. Pode representar sério risco para quem o manipula e risco à comunidade. Existe medida de tratamento e/ou de prevenção. Na maioria dos casos, de alto potencial de contaminação por aerossóis;
-
Classe 4 - Microrganismo patogênico que ponham em risco a vida do homem ou de espécie animal por inexistência de tratamento ou prevenção. Representando grande risco a quem o manipula e tendo grande poder de disseminação de um indivíduo a outro. A transmissão se dá por aerossóis ou por outra forma desconhecida de transmissão.
Recomendações de biossegurança em biotério de experimentação
Existem quatro níveis de biossegurança, crescente em função do grau de contenção e complexidade do nível de proteção.
O nível de biossegurança de um experimento é determinado segundo o microrganismo de maior risco. A seleção do nível apropriado de biossegurança para o trabalho com um determinado agente ou em experimentos com animais, depende de inúmeros fatores. Alguns mais importantes são: a virulência, a patogenicidade, a estabilidade biológica, o meio de propagação, a natureza e função do laboratório, os procedimentos e manipulações envolvendo o agente, a endemicidade do agente e a existência de vacina ou medidas terapêuticas efetivas.
Os biotérios de experimentação como os laboratórios de microbiologia, devem ser projetados de acordo com o grupo de risco dos agentes que serão trabalhados e sobre a visão das recomendações de biossegurança para os níveis 1, 2, 3 e 4. Outros fatores devem ser levados em consideração, em função da particularidade de cada laboratório e/ou biotério. Em relação aos animais, deve-se considerar sua agressividade e tendência de morder, ou arranhar; os ectoparasitos e endoparasitos que possam estar presentes; as zoonoses que são susceptíveis e a possibilidade de disseminação de alérgenos.
Os procedimentos e práticas que devem ser consideradas no desenvolvimento de atividades que envolvam animais vertebrados e em função do nível de biossegurança estão descritos a seguir.
Orientações preconizadas para biotérios de experimentação
Procedimentos e práticas:
Níveis 1, 2, e 3
O acesso é limitado ou restrito ao critério da chefia. Recomenda-se que não seja permitido o acesso às salas de animais e áreas onde são manipulados animais e materiais que tiveram contatos com os animais ou seus dejetos gestantes, crianças, de outras pessoas que não tenham atividades a desenvolver no biotério ou que não estejam devidamente imunizadas;
As mãos devem ser higienizadas, sempre que possível, após remover as luvas e antes de sair do ambiente de manipulação, bem como antes de sair do biotério;
Não é permitido nas áreas de animais comer, beber, fumar, guardar comida, usar cosméticos, manipular lentes de contato.

Fig 5. Sinalização de proibido comer
As portas devem abrir para o interior das áreas de maior risco e devem, sempre que possível, possuir molas para que não permaneçam abertas;
O combate a insetos, roedores e demais animais indesejáveis devem ser efetivo e regular.
Níveis 2, e 3
Todas as recomendações para o nível 1 mais:
-
Evitar movimentos bruscos, de forma a evitar a formação de aerossóis.
-
As áreas, bancadas e equipamentos devem ser desinfetadas após o uso ou quando da contaminação com material patogênico;

Fig 6. Higienização de ambiente
-
Os materiais, resíduos e lixos provenientes das áreas de animais são descontaminados, mas é preferível que sejam esterilizados por autoclave, e após esse procedimento podem ser considerados lixo comum. As carcaças infectadas são incineradas.
-
As gaiolas de animais devem ser descontaminadas por autoclave, antes de serem enviadas para a área de higienização, quando se fará a retirada de dejetos e material de forração e posterior lavagem;
Nível 4
Todas as recomendações para os níveis 1, 2 e 3, mais:
Equipamentos e bancadas de trabalho devem ser desinfetadas regularmente e logo após o trabalho com patógenos e imediatamente após a contaminação acidental com material patogênico. Equipamentos contaminados devem ser desinfetados antes de retirado das instalações.
Procedimentos e práticas específicas
Nível 1
Deve haver um responsável pela liberação de acesso de pessoas às áreas de animais e áreas com risco biológico. As pessoas devem ser informadas dos potenciais riscos.
Pessoas adoentadas ou com baixa resistência imunológica não devem ter acesso às áreas de animais.
Normas e procedimentos devem ser elaborados de forma que as pessoas tomem conhecimento dos riscos específicos e procedimentos a serem adotados.
O material utilizado como “cama” para os animais e que forram as gaiolas deve ser manuseado cuidadosamente de forma a evitar a criação de aerossóis.
 |
 |
Figs 7 e 8 – Cabine de descarte de rejeitos
As gaiolas podem ser lavadas sem nenhuma recomendação específica, porém o uso de água quente auxilia na redução da flora microbiológica presente nesses materiais.
Recomenda-se que as roupas sejam apropriadas e exclusivas de uso no biotério.
Deve haver um manual que contemple as questões de biossegurança e que esse seja de conhecimento de todos. Todos devem praticar as recomendações desse manual.

Fig 9. Manuais de biossegurança / Fiocruz
Nível 2
Todas as recomendações para os níveis 1, mais:
-
Quando do uso de agentes patogênicos nas salas de animais, devem estar disponíveis equipamentos de proteção individual para acesso a essas salas, como por exemplo óculos ou visor de proteção, máscaras com elemento filtrante, etc.
-
Na porta de acesso deve haver um aviso com o símbolo de biossegurança, onde identifique o agente de risco, responsáveis, telefones de contato e equipamentos de uso obrigatório;

Fig 10. Aviso de risco
-
Todas as pessoas devem ser imunizadas contra a doença específica, caso exista vacina;
-
Sorologia periódica das pessoas envolvidas deve ser realizada em função do patógeno;
-
Todas as pessoas devem ter treinamento em aspectos de biossegurança e, em especial, aos relativos ao agente em estudo. Esse treinamento deve ser reforçado anualmente e sempre que houver mudanças de procedimentos ou práticas;
-
Materiais contaminados deve ser objeto de cuidados especiais, principalmente os perfurocortantes. Esses devem ser exclusivos às áreas de animais e usados somente quando não houver método alternativo;
-
Nunca se deve reencapar as agulhas hipodérmicas com o risco de puncionar os dedos, bem como não devem ser manipuladas com as mãos após desprezadas ou quando caem sobre a bancada ou chão. Nesse e no caso de frascos de vidro quebrados utilizar pinça para recolhê-los. Os perfurocortantes devem ser desprezados em caixas apropriadas, de parede rígidas e impermeáveis.

Fig 11. Recipiente para descarte de perfurocortantes
-
Os cultivos celulares, culturas bacterianas e tecidos são acondicionados em caixas apropriadas, de paredes sólidas e impermeáveis nos processos de coleta, estocagem e transporte;
-
Acidentes com material patogênico são comunicados ao responsável para que este possa providenciar os cuidados pertinentes e registros, bem como encaminhamento médico;
-
Animais que não estejam relacionados ao experimento não devem ser admitidos no biotério.
Nível 3
Todas as recomendações para os níveis 1 e 2, mais:
-
Não devem ter acesso ou trabalhar nesse nível de risco gestante, imunodeficientes ou imunodeprimidos e crianças.
-
Todas as pessoas são informadas sobre os potenciais riscos e orientadas de como agir para sua proteção e da coletividade.
-
As pessoas ao saírem da área de animais deverão retirar a paramentação em local próprio e as colocar em recipiente específico para ser encaminhada à esterilização. Essa paramentação deve ser composta de tantas peças quanto necessárias a fim de recobrir todo o corpo do técnico, compondo-se de blusa, calça, calçado, gorro, máscara, meia e luva apropriada à espécie animal em questão. Todos fazem uso dessa paramentação nas áreas de animais. Na saída, se retira a paramentação antes do banho obrigatório;
-
Todo lixo e materiais provenientes das áreas de animais são autoclavados, As carcaças de animais são incineradas. O transporte de animais para o incinerador é feito em caixa apropriada, de paredes rígidas e impermeáveis.
Nível 4
Todas as recomendações para os níveis 1, 2 e 3, mais:
-
Só os técnicos com atividades específicas nos trabalhos em andamento podem entrar nessa área. As pessoas debilitadas imunologicamente não podem entrar nessas instalações. Crianças, gestantes, imunideficientes ou imunodeprimido não devem ter acesso às áreas de risco.
-
A entrada ao biotério deve ter segurança para o controle de acesso de pessoas.
-
Deve haver o estabelecimento de um procedimento operacional para situações emergenciais;
-
Seringas e agulhas hipodérmicas são usadas somente para situações que não aja método alternativo, como sangria e inoculações.
-
As pessoas ao entrarem e saírem deverão fazer obrigatoriamente a troca de roupas e o banho na saída.
-
Materiais, insumos e outros produtos devem ser descontaminados ou esterilizados em “airlock”, antecâmara ou autoclave dupla-porta, antes de introduzidos na área de animais;
-
Deve haver um programa de emergência para casos de acidentes e contaminação com patógenos, bem como verificação de ausência de pessoal.
-
O suporte médico deve ser implantado, principalmente, para doenças associadas ao trabalho/pesquisa. Nessas instalações deve haver uma área específica à quarentena, isolamento e cuidados médicos para técnicos suspeitos ou com doença associada à atividade;
Bibliografia
-
Canadian Council on Animal Care – Guide to the Care and Animal Use of Experimental, Vol I and II. 1984
-
Center for Disease Control and Prevention e National Institutes of Health. 1993. Biosafety in Microbiological and Biomedical Laboratories. 3rd ed. HHS publication n° 93-8359 (CDC). Washington, D.C. U.S. Government Printing Office.
-
Colégio Brasileiro de Experimentação Animal / COBEA – Manual para Técnicos em Bioterismo, 1996.
-
Comissão Técnica Nacional de Biossegurança, Instrução Normativa n0 2, Dispõe sobre a classificação de riscos de Organismos Geneticamente Modificados (OGM) e os níveis de biossegurança a serem aplicados nas atividades e projetos com OGM e seus derivados em contenção
-
Clough,G. and Gamble, M.R. – Medical Research Council – Laboratory Animal Center -Laboratory Animal House, 1976.
-
Guide to de care and Use of Laboratory Animal. 1996. National Research Council.
-
Majerowicz. J. Boas Práticas em Biotérios e Biossegurança. Rio de Janeiro: Interciência. 2008, v.1. p.173
-
Majerowicz. J. Formas para Controlar a Alergia em Biotérios. Controle de Contaminação. , v.53, p.34 - 38, 2003.
-
Molinaro, E; Majerowicz, J; Valle S. Biossegurança em Biotério. Rio de Janeiro: Interciência, 2007, v.1. p.226.
-
National Academy of Science – Support Personel for Animal Research, 1969. National Research Council. 1999. Guia para el Cuidado y Uso de los Animales de Laboratório. NW, Washington, 146 p.
-
Organización Mundial de la Salud – Guia para el Transporte Seguro de Substancias Infecciosas y Especímenes Diagnósticos, 1997.
-
Seamer, J.H. and Wood, M. – Safety in the Animal House, 1981.
-
World Health Organization, Laboratory Biosafety Manual – Second Edition. U.S. Department of Health, Education and Welfare (1997) – Guide for the care and Use of laboratory Animal.
 Joel Majerowicz MV MSc. Médico Veterinário, graduado pela Universidade Federal Rural do Rio de Janeiro (1981). Especialização em criação de animais livres de microrganismos patogênicos específicos no Institute of Veterinary Medicine, Alemanha (1988). Mestre em Tecnologia em Imunobiológicos pela Fundação Oswaldo Cruz – Fiocruz (2005). Chefe do Serviço de Criação de Roedores, Lagomorfos, Ovinos e Equinos do Departamento de Biotérios do Instituto de Tecnologia em Imunobiológicos / Fiocruz: 1988 a 1995. Chefe do Laboratório de Experimentação Animal (LAEAN) de Bio-Manguinhos / Fiocruz: 1996 a 2007. Gerente do projeto do Centro Integrado de Protótipos, Biofármacos e Reativos para Diagnóstico (CIPBR) / Bio-Manguinhos / Fiocruz: 2007 a 2009. Diretor do Centro de Criação de Animais de Laboratório (Cecal) / Fiocruz: 2009 a 2013. Assessor para biotérios e biossegurança no Centro de Desenvolvimento Tecnológico em Saúde (CDTS) / Fiocruz (2013). Coordenador do Curso de Atualização Profissional em Biossegurança em Biotérios da Escola Politécnica de Saúde Joaquim Venâncio / Fiocruz. Organizador do livro Biossegurança em Biotérios (Molinaro, Majerowicz & Valle, 2008). Autor do livro Boas Práticas em Biotérios e Biossegurança (Majerowicz, 2008).
Joel Majerowicz MV MSc. Médico Veterinário, graduado pela Universidade Federal Rural do Rio de Janeiro (1981). Especialização em criação de animais livres de microrganismos patogênicos específicos no Institute of Veterinary Medicine, Alemanha (1988). Mestre em Tecnologia em Imunobiológicos pela Fundação Oswaldo Cruz – Fiocruz (2005). Chefe do Serviço de Criação de Roedores, Lagomorfos, Ovinos e Equinos do Departamento de Biotérios do Instituto de Tecnologia em Imunobiológicos / Fiocruz: 1988 a 1995. Chefe do Laboratório de Experimentação Animal (LAEAN) de Bio-Manguinhos / Fiocruz: 1996 a 2007. Gerente do projeto do Centro Integrado de Protótipos, Biofármacos e Reativos para Diagnóstico (CIPBR) / Bio-Manguinhos / Fiocruz: 2007 a 2009. Diretor do Centro de Criação de Animais de Laboratório (Cecal) / Fiocruz: 2009 a 2013. Assessor para biotérios e biossegurança no Centro de Desenvolvimento Tecnológico em Saúde (CDTS) / Fiocruz (2013). Coordenador do Curso de Atualização Profissional em Biossegurança em Biotérios da Escola Politécnica de Saúde Joaquim Venâncio / Fiocruz. Organizador do livro Biossegurança em Biotérios (Molinaro, Majerowicz & Valle, 2008). Autor do livro Boas Práticas em Biotérios e Biossegurança (Majerowicz, 2008).


















Comentarios
Bom Dia,
Gostaria de tirar uma dúvida, pois não estou conseguindo achar em nenhum artigo da área. Quando uma pessoa trabalha em uma área com animais em microisolador duas vezes na semana e necessita trabalhar os outros três dias em uma área SPF quais seriam os critérios utilizados com relação a contaminação? Seria suficiente o banho e troca de vestimenta?
Grata Bianca
Bom dia Dr. Joel.
Gostaria de sua opinião sobre o bem estar gerado pelo substrato XILANA, produto adquirido pela granulação de sabugo de milho em tamanho adequado ao tipo do animal, Ratos ¼” e Camundongo 1/8”.